Hämatologie und internistische Onkologie in Oberhausen und Dinslaken
Dr. Heike Steiniger, Axel Schneider, Dr. Julia Baum, Dr. Maria Sakarou,
Bahnhofstr. 64, 46145 Oberhausen
Kreuzstr. 28, 46535 Dinslaken


Häufige Fragen zur Onkologie und Hämatologie
Was ist Onkologie und Hämatologie?
Die Onkologie beschäftigt sich mit der Behandlung bösartiger solider Tumore, also Darmkrebs, Lungenkrebs, Brustkrebs, Prostata-Karzinom uvm.. In der Hämatologie geht es zum einen um bösartige Tumore der blutbildenden Zellen wie Leukämien und Lymphome und auch um nicht tumorbedingte Blutbildveränderungen, die angeboren sein können oder auch durch einen Mangel an Eisen, Vitaminen oder im Rahmen anderer Erkrankungen auftreten.
Der Facharzt für Hämatologie und internistische Onkologie ist derjenige, der sich hauptberuflich mit der Diagnose und Therapie der oben genannten Erkrankungen beschäftigt.
Tumorerkrankungen werden immer häufiger - woran liegt das?
Die meisten Tumorerkrankungen treten - gerechnet auf das Alter - nicht häufiger auf als früher. Das Magen-Karzinomen war in den 1930er Jahren in den USA noch die häufigste Krebs-Todesursache und hat seitdem auch in Deutschland u.a. durch verbesserte Konservierungstechniken bei Lebensmitteln um etwa den Faktor 8 abgenommen. Da aber die meisten Tumorerkrankungen (glücklicherweise) in eher höherem Lebensalter auftreten und immer mehr Menschen ein höheres Lebensalter erreichen, weil z.B. Herz-/Kreislauferkrankungen in den letzten Jahrzehnten zunehmend besser behandelt werden, nimmt die Zahl an Tumorneuerkrankungen in Absolutzahlen deutlich zu, bei Männern z.B. im Vergleich zu 1980 um 90%.
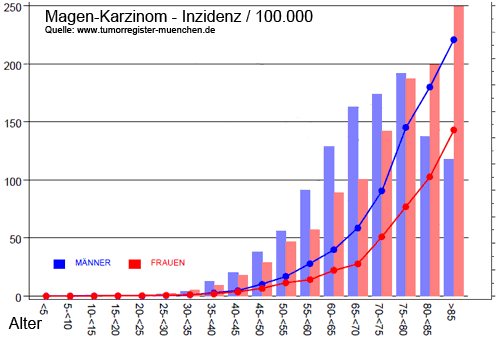 Das Risiko innerhalb eines Jahres eine Tumorerkrankung zu bekommen ist für einen 80 Jährigen im Vergleich zu einem 15 Jährigen etwa 200 bis 300x höher, daran zu versterben sogar um den Faktor 1000.
Das Risiko innerhalb eines Jahres eine Tumorerkrankung zu bekommen ist für einen 80 Jährigen im Vergleich zu einem 15 Jährigen etwa 200 bis 300x höher, daran zu versterben sogar um den Faktor 1000.
Die Zunahme von Tumorerkrankungen ist also kein Zeichen für eine zunehmende Belastung durch Ernährung, Umweltgifte, Beruf o.a. sondern ganz im Gegenteil ein Zeichen für eine bessere Gesundheit und ein längeres Leben. Wenn Männer in den 1970er-Jahren häufig mit Ende 50/Anfang 60 am Herzinfarkt gestorben sind, konnten sie mit 70 Jahren keine Tumorerkrankung mehr bekommen.
Außerdem können viele Tumorerkrankungen besser behandelt werden als z.B. vor 30 Jahren, so dass es auch dadurch immer mehr Menschen gibt, die von einer Tumorerkrankung geheilt wurden oder mit einer Tumorerkrankung leben.
Aktuell erkranken etwa eine halbe Million Menschen in Deutschland pro Jahr neu an Krebs und bei etwa 1,5 von 80 Millionen in Deutschland lebenden Menschen ist die Tumordiagnose weniger als 5 Jahre her.
Sind Tumorerkrankungen heilbar?
Insgesamt - also günstige und weniger günstige, frühe und fortgeschrittene Stadien bei Erstdiagnose zusammen genommen - werden mehr als die Hälfte der Menschen von einer bösartigen Tumorerkrankung geheilt bzw. sterben nicht an der Erkrankung. Bei der Mehrheit der häufigen Tumorerkrankungen (Brust-, Dickdarm-, Gebärmutterhalskrebs u.a.) die in einem sehr frühen Stadium entdeckt werden, können 90% oder mehr der Betroffenen durch eine Operation, Bestrahlung und/oder eine Chemotherapie geheilt werden.
Bei einigen wenigen Tumorerkrankungen (Hodentumoren, Lymphomen, Schilddrüsenkarzinomen, wenigen Lebermetastasen bei Dickdarmtumoren u.a.) ja. Bei der Mehrheit der sog. soliden Tumore wie Lungenkrebs oder Brustkrebs ist eine Heilung in der Regel nicht mehr möglich, wenn Metastasen aufgetreten sind, sehr wohl aber eine Behandlung und ein Leben mit der Tumorerkrankung. 
Auch eine Zuckererkrankung oder ein Herzinfarkt durch Gefäßverkalkung ist nicht heilbar und muss lebenslang behandelt werden. Viele Menschen leben aber viele Jahre mit häufig nur geringen Einschränkungen mit Zucker oder nach einem Infarkt. Das gelingt
durch mehr und besser verträgliche Therapien auch zunehmend bei vielen Tumorerkrankungen, wenn auch häufig noch nicht so lange wie bei Diabetes oder Arteriosklerose.
Sind Tumorerkrankungen vererbbar?
Mehrheitlich nein. Zu Tumorerkrankungen kommt es meist, weil im Laufe des Lebens verschiedene vermeidbare oder auch unvermeidbare Ereignisse wie z.B. die normale Belastung durch die Umwelt, Rauchen uvm. zusammen gekommen sind, die dann zu einer Tumorerkrankung geführt haben. Einige wenige Tumorerkrankungen sind erblich. Beispielsweise findet man bei etwa 5-10% der Frauen mit Brustkrebs eine genetische Veränderung (BRCA1/2, CHEK2 u.a.), die gleichzeitig auch das Risiko an anderen Tumoren wie Eierstock-, Darm-, Bauchspeicheldrüsen-Krebs und Lymphomen zu erkranken erhöhen kann. Betroffen sind in diesen Fällen meist Gene, die für die Reparatur von natürlich vorkommenden Schäden an der Erbsubstanz zuständig sind.
Kann ich mein Tumorrisiko z.B. durch Ernährungsumstellung oder Nahrungsergänzungsmittel senken?
Abgesehen von zuviel Alkohol oder einem erheblichen Übergewicht spielt der beeinflussbare Teil der Ernährung eine weniger große Rolle als allgemein angenommen. Mit dem Verzicht auf Zucker in der Nahrung lässt sich kein Tumor - außer im Reagenzglas - am Wachstum hindern. Insbesondere gibt es im Moment kein Vitamin oder Spurenelement, das erwiesenermaßen zu einer Reduktion des Tumorrisikos führt oder gar eine Tumorzelle wieder dazu bringen kann, sich wieder wie eine normale Zelle zu verhalten. Ganz im Gegenteil hat man z.B. bei erhöhter Zufuhr von einigen Vitaminen ein vermehrtes Auftreten von Tumorerkrankungen beobachtet. 
Raucher sollten beispielsweise kein Vitamin A zusätzlich zu sich nehmen. Wenn Sie Rauchen, können Sie aber als wirkungsvollste Maßnahme mit dem Einstellen des Rauchens eine ganz erhebliche Reduktion Ihres Tumorrisikos nicht nur für Lungenkrebs erreichen.
Informationen zu Vorsorgeuntersuchungen wie Darmspiegelung, gynäkologische und urologische Vorsorge, Hautkrebsscreening u.a. finden Sie bei den jeweiligen Fachrichtungen.
Kann man nachdem ein Tumor operiert wurde noch zusätzlich etwas tun?
Bei einigen Tumoren wird häufig noch zusätzlich vor- oder nach einer Operation bestrahlt (insbesondere bei Brustkrebs, Rektumkarzinomen, Lungenkrebs u.a.), um die Kontrolle am Ort der Operation bzw. der Umgebung zu verbessern.
Bei den meisten häufigen Tumoren ist abhängig vom Tumorstadium das Risiko
hoch, dass sich schon vor einer Operation Tumorzellen abgelöst und über die Blutbahn oder die Lymphwege verteilt haben. Diese winzigen Absiedelungen lassen sich nicht darstellen oder beweisen, auch nicht durch eine Computer- oder Kernspintomographie (CT/MRT) oder ein PET. Bei einem Dickdarmtumor mit Absiedelungen in den lokalen Lymphknoten weiss man beispielsweise, dass der Tumor wenn man nichts nach der Operation machen würde bei etwa jedem 2. Menschen in der Leber, Lunge oder an anderer Stelle wiederkommen würde. Durch eine Infusions-Chemotherapie (die keine Übelkeit macht und in der Regel auch nicht zu Haarausfall führt), lässt sich dieses Risiko etwa halbieren. Eine solche Therapie wird adjuvante = Sicherheits-Chemotherapie genannt.
In den Medien hört man von einer besonders genauen Bestrahlungsmethode die z.B. in Heidelberg angeboten wird. Könnte mir das weiterhelfen?
Die übliche Bestrahlung wird aktuell mit Röntgenstrahlen (Photonen) durchgeführt, die mit Hilfe eines Linearbeschleunigers mit hoher Energie erzeugt werden. Meist wird vorher ein Planungs-CT durchgeführt und durch eine Computerplanung genau berechnet, über welche Felder wie bestrahlt werden muss, damit das Zielgebiet die gewünschte Dosis bekommt und das umgebende Gewebe bestmöglich geschont wird.
Bei den meisten Tumoren ist das oben genannte Verfahren das günstigste, gerade weil auch in der unmittelbaren Umgebung des Tumors, wo sich Tumorzellen z.B. in Lymphspalten befinden können, noch eine relativ hohe und zum Abtöten der Tumorzellen ausreichende Strahlendosis erreicht wird. Das gilt z.B. für die Bestrahlung von Knochen, der Brust, des Kopfes, von Lungentumoren uvm..
Es gibt seit geraumer Zeit mehrere Methoden, die Strahlendosis stärker auf das Zielvolumen zu konzentrieren. Dazu gehört zum einen die stereotaktische Bestrahlung.
Die älteste und bekannteste Methode ist das Gamma-Knife, das häufig bei der Bestrahlung von einer einzelnen oder einigen wenigen Hirnmetastasen oder auch bei gutartigen Hirntumoren angewandt wird. Dabei wird ein Zielkranz aus Metall am Schädelknochen befestigt und über ca. 200 einzelne Kobalt-Quellen ein (oder einige wenige) Zielvolumen sehr genau mit einer sehr hohen Dosis bestrahlt. Das nächstgelegene Gamma-Knife Zentrum von Oberhausen aus liegt in Krefeld.
Auch mit einem Linearbeschleuniger lässt sich sehr zielgenau bestrahlen. Bei Kopftumoren erfolgt dies ähnlich wie beim Gamma Knife mit einer aufwändigeren Ziel- und Planungstechnik.
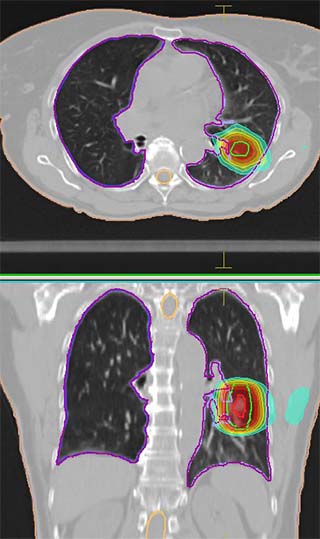
Eine neuere Technik ist die Intensitätsmodulierte Strahlentherapie (IMRT), bei der über eine noch größere Zahl an Feldern und mit sich während der Bestrahlung veränderbaren Feldgrenzen bestrahlt wird. Dadurch wird ein stärkerer Abfall der Strahlendosis in der Umgebung erreicht. Dieses Verfahren ist außer bei Tumoren im Kopfbereich auch zum Teil bei Prostata-Karzinomen, einigen Tumoren im Kopf-Hals-Bereich und wenn sehr strahlenempfindliche Gewebe benachbart liegen etabliert.
Die aktuellen Berichte über Neubauten in den Medien betreffen meist Bestrahlung nicht mehr mit Röntgenstrahlen sondern mit geladenen Atomkernen wie Protonen (im Bau z.B. in Essen) oder mit Schwerionen (in Heidelberg) z.B. Kohlenstoff. Diese im Vergleich mit Photonen sehr großen Teilchen haben gewisse physikalische Vorteile, wenn eine höhere Eindringtiefe und ein starker Dosisabfall dahinter gewünscht sind. Behandelte Tumoren betreffen aktuell die Schädelbasis, einige Sarkome, einige besondere Kopf-Hals-Tumore und Prostata-Karzinome.
Der Vorteil aller gezielten Therapieverfahren ist auch deren Nachteil. Wie oben genannt, wird das Gewebe in der Umgebung weniger bestrahlt. Damit sind Tumore, bei denen die Bestrahlung Ausläufer in das umgebende Gewebe abtöten soll, weniger geeignet. Dies trifft auf die Mehrheit der soliden Tumore zu. Außerdem ist eine sehr aufwändige Tumorlokalisation während der Bestrahlung notwendig, weil sich z.B. die Prostata-Lage abhängig von der Füllung des Enddarms täglich und mitunter sogar während der Bestrahlung ändern kann. Unter ungünstigen Umständen würde eine gezielte Bestrahlung ohne Lagekontrolle sonst einen Teil des Tumors nicht mehr ausreichend treffen.
In der Zeitung wird von einer zielgerichteten Therapie durch eine Genanalyse z.B. bei Lungenkrebs durch die Uniklinik Köln berichtet. Kann ich das auch bekommen?
Bei einigen Tumoren lässt sich durch eine Analyse der Gen- oder Proteinstruktur der Tumorzellen erkennen, ob eine bestimmte Therapie wirken kann oder nicht. Das bekannteste Beispiel dafür ist die (meist vorhandene) Ausprägung von Hormonrezeptoren bei Brustkrebs. Wenn der Tumor die hat, kann eine antihormonelle Therapie eingesetzt werden. In den letzten Jahren ist auch bei anderen Tumoren eine Vielzahl von Genveränderungen und den daraus meist resultierenden unterschiedlichen Ausprägungen von Proteinen festgestellt worden.
Gegen einen Teil dieser Veränderungen, gibt es inzwischen schon Medikamente, gegen viele andere aber noch nicht. Alle Merkmale gegen die es schon Medikamente gibt, werden routinemäßig auch außerhalb von Forschungsvorhaben bei uns getestet und die entsprechenden Medikamente gegeben.
Die bekanntesten Beispiele dafür sind die Her2-Expression bei Brustkrebs für die Therapie mit Trastuzumab/Lapatinib/ Pertuzumab/Trastuzumab-Emtansin oder die Bestimmung der KRAS/NRAS Veränderungen für die Therapie bei colorektalen Karzinomen mit Cetuximab/Panitumumab.
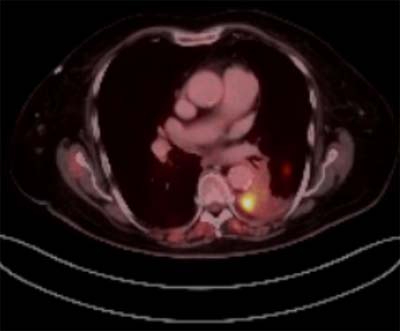 Bei Lungenkrebs gab es bis vor einigen Jahren wenig Fortschritte, so dass die Entdeckung neuer Behandlungswege ausgesprochen zu begrüßen ist. Dies hat schon Ende der 90er Jahre zur Entwicklung von Medikamenten gegen ein das Zellwachstum regulierendes Enzym - die EGF-Rezeptor-Thyrosin-Kinase - geführt (EGF=Epidermal Growth Factor=epidermaler Wachstumsfaktor). Anfangs wurden diese Medikamente aber unselektiert allen Menschen mit Lungenkrebs gegeben. So gegeben half es bei relativ wenigen Patienten sehr gut aber es traten bei einigen Menschen schwerwiegende Nebenwirkungen auf, was die Zulassung des ersten Medikaments Gefitinib/ZD1839 erheblich verzögert hat. Das zweite Medikament Erlotinib wurde schon 2005 zugelassen. Erst gut 10 Jahre nach den ersten Studien hat man nachgewiesen, dass die sehr gute Wirkung fast ausschließlich bei Tumoren auftritt, die eine Veränderung (Mutation) im EGF-Rezeptor-Gen haben, die zu einer dauerhaften Aktivierung des Rezeptors führt. Das kann man sich so vorstellen, als ob z.B. der Insulin-Rezeptor auch ohne Insulin immer aktiv wäre. Bei einer aktivierenden Mutation des EGF-Rezeptors kommt es dadurch zu einem Wachstum von Lungentumoren. Inzwischen gibt es auch noch weitere Medikamente wie Afatinib die noch wirken können, wenn eine Mutation aufgetreten ist, gegen die Gefitinib oder Erlotinib nicht wirken.
Bei Lungenkrebs gab es bis vor einigen Jahren wenig Fortschritte, so dass die Entdeckung neuer Behandlungswege ausgesprochen zu begrüßen ist. Dies hat schon Ende der 90er Jahre zur Entwicklung von Medikamenten gegen ein das Zellwachstum regulierendes Enzym - die EGF-Rezeptor-Thyrosin-Kinase - geführt (EGF=Epidermal Growth Factor=epidermaler Wachstumsfaktor). Anfangs wurden diese Medikamente aber unselektiert allen Menschen mit Lungenkrebs gegeben. So gegeben half es bei relativ wenigen Patienten sehr gut aber es traten bei einigen Menschen schwerwiegende Nebenwirkungen auf, was die Zulassung des ersten Medikaments Gefitinib/ZD1839 erheblich verzögert hat. Das zweite Medikament Erlotinib wurde schon 2005 zugelassen. Erst gut 10 Jahre nach den ersten Studien hat man nachgewiesen, dass die sehr gute Wirkung fast ausschließlich bei Tumoren auftritt, die eine Veränderung (Mutation) im EGF-Rezeptor-Gen haben, die zu einer dauerhaften Aktivierung des Rezeptors führt. Das kann man sich so vorstellen, als ob z.B. der Insulin-Rezeptor auch ohne Insulin immer aktiv wäre. Bei einer aktivierenden Mutation des EGF-Rezeptors kommt es dadurch zu einem Wachstum von Lungentumoren. Inzwischen gibt es auch noch weitere Medikamente wie Afatinib die noch wirken können, wenn eine Mutation aufgetreten ist, gegen die Gefitinib oder Erlotinib nicht wirken.
Die zweite Zielstruktur bei Lungentumoren, gegen die es schon ein allgemein erhältliches Medikament (seit 10/2012 Crizotinib, demnächst auch Ceritinib u.a.) gibt, ist das Enzym das durch die Veränderung des ALK-Gens (ALK=Anaplatische Lymphom Kinase) entsteht oder noch seltener ROS1.
Den o.g. Genveränderungen - EGF, ALK und ROS1 - ist gemein, dass sie hauptsächlich bei Adenokarzinomen der Lunge bei Nichtrauchern und dort auch nicht bei allen zu finden sind, also insgesamt bei deutlich weniger als 10% aller Patienten mit Lungentumoren.
Eine andere neue Therapiemethode, die über die EInwirkung auf Regulationspunkte des Immunsystems (PD-1, PD-L1) wirkt, könnte
auch gegen die bei Rauchern häufigeren Plattenepithelkarzinome hilfreich sein.
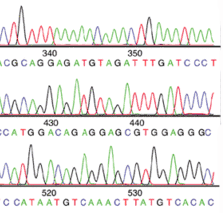 Während noch vor gut 10 Jahren Genuntersuchungen nach der Snager-Methode ähnlich wie nebenstehend aussahen (Quelle: genome.gov) und sehr aufwändig und teuer waren, wurde durch die Entwicklung verbesserter schneller Untersuchungsmethoden (Schlagwort NGS=next generation sequencing) die preiswertere Untersuchung auch umfangreicher Gensammlungen in der Routinediagnostik möglich.
Während noch vor gut 10 Jahren Genuntersuchungen nach der Snager-Methode ähnlich wie nebenstehend aussahen (Quelle: genome.gov) und sehr aufwändig und teuer waren, wurde durch die Entwicklung verbesserter schneller Untersuchungsmethoden (Schlagwort NGS=next generation sequencing) die preiswertere Untersuchung auch umfangreicher Gensammlungen in der Routinediagnostik möglich.
An der Uniklinik in Köln aber auch in Essen und vielen anderen Stellen werden schon seit einigen Jahren Lungentumore systematisch auf verschiedene Genveränderungen untersucht. Die Uniklinik Köln hat hier die aktivste Pressearbeit und eine Kooperation mit der AOK Rheinland/Hamburg, durch die Patienten der Kasse ihren Tumor dort untersuchen lassen können. Als Forschungsvorhaben sind solche Untersuchungen wie oben schon ausgeführt ausgesprochen hilfreich für die Entwicklung neuer Substanzen, bringen individuell einem Patienten der jetzt einem Lungentumor hat, der schon auf die Wirksamkeit von vorhandenen Medikamenten getestet wurde, häufig keine akut hilfreiche Aussage.
Das Ergebnis eines solchen Test sieht - wenn sich denn eine zusätzliche Mutation findet - beispielsweise wie folgt aus (Wildtyp=nicht verändertes Gen):
| Gen | Exon | Mutationsstatus | Frequenz % | Interpretation | Therapieoption |
|---|---|---|---|---|---|
| AKT1 | 4 | Wildtyp | |||
| ALK | 21-25 | Wildtyp | |||
| BRAF | 11,15 | Exon11 Mutation | 10% | inaktivierend | keine |
| CTNNB1 | 3 | Wildtyp | |||
| DDR2 | 3-18 | Wildtyp | |||
| EGFR | 18,19,21 | Wildtyp | |||
| EGFR | 20 | Wildtyp | |||
| Her2 | 19,20 | Wildtyp | |||
| KRAS | 2,3 | Wildtyp | |||
| MAP2K1 | 2 | Wildtyp | |||
| MET | 14 | Wildtyp | |||
| NRAS | 2,3 | Wildtyp | |||
| PIK3CA | 9,20 | Exon 9 Mutation | 5% | aktivierend | Studie prüfen |
| PTEN | 1-8 | Wildtyp | |||
| TP53 | 5-8 | Wildtyp |
- Wildtyp = keine (bisher bekannte) Veränderung bedeutet, dass es hier keinen Therapieansatz gibt.
- Inaktivierende Mutation bedeutet, dass es meist entweder keinen Therapieansatz gibt oder wie z.B. bei
KRAS/NRAS bei Dickdarmtumoren eine Therapie nicht gemacht werden sollte.
- Aktivierende Mutation bedeutet, dass es einen möglichen Therapieansatz gibt, aber außer bei EGFR und ALK die schon zuvor getestet wurden kein zugelassenes Medikament für Lungentumore..
Im oben genannten Fall gibt es zwar einen jetzt aktuell neu zugelassenen Phosphatidylinositol-3-Kinase (PI3K)Hemmer (Idelalisib), der aber nur bei Lymphomen speziell der chronischen lymphatischen Leukämie hilft. Andere PI3K-Hemmer sind zwar in Entwicklung, haben aber ebenso wie andere schon länger bekannte Hemmer des gleichen Signalweges (PIK3-AKT-mTOR) bisher eher eine Bedeutung bei hämatologischen Erkrankungen.
An Studien für Lungentumore gab es hier
zum Zeitpunkt des Befundes in Deutschland eine Phase-II-Studie mit Docetaxel+/-Buparlisib bei Plattenepithel-Karzinomen (der Tumor war aber ein Adeno-CA) und eine Studie mit GDC-0941/Pictilisib für unvorbehandelte Patienten, der Tumor war aber vorbehandelt. Keine der Studien hatte einen Studienort in NRW.
Zusammenfassend: wenn Ihre Krankenkasse es anbietet oder sich im Rahmen einer Studie die Gelegenheit ergibt, lassen Sie ihren Tumor untersuchen. Sie sollten aber nicht enttäuscht sein, wenn sich daraus meist keine akute Behandlungsmöglichkeit ergibt. In der Presse klingt das in der Kurzfassung in der Regel anders.
Sind Bluttransfusionen schädlich ("Böses Blut")?
In der ARD lief kürzlich eine Sendung, die mit z.T. dramatischen Worten vor Bluttransfusionen gewarnt und entsprechende Nachfragen und Verunsicherung bei vielen Patienten ausgelöst hat. Der Begleittext zur Sendung gibt die Lage deutlich realistischer wieder: bei sehr niedrigen Werten für den roten Blutfarbstoff Hämoglobin (Hb), sei es akut durch eine Verletzung, eine Operation mit sehr hohem Blutverlust oder eine Erkrankung, rettet eine Bluttransfusion das Leben und der Nutzen überwiegt die Risiken erheblich.
Richtig ist auch, dass Alternativen für eine Bluttransfusion bedacht werden sollten. Operationen sollten möglicht transfusionssparend durchgeführt werden und bei geplanten Eingriffen sollten Möglichkeiten zur Anhebung des Hämoglobinwertes wie z.B. Eisen-Infusionen genutzt werden. Diese Erkenntnisse sind nicht wirklich neu, werden aber verschieden intensiv verfolgt. Eine Förderung solcher Aktivitäten ist zu begrüßen.
In der o.g. Sendung wurde aber insbesondere auch bei Tumorpatienten vor Bluttransfusionen gewarnt, weil sie das Immunsystem schwächen könnten. Dass Bluttransfusionen insbesondere wenn sie häufiger gegeben werden einen Einfluss auf das Immunsystem haben, ist seit vielen Jahrzehnten bekannt.
Bevor es wirksame Medikamente zur Immun-Unterdrückung nach Nierentransplantationen gab hatte man nachgesehen, bei welchen Patienten eine transplantierte Niere besonders gut und lang angenommen worden war. Das waren die Patienten mit vielen Bluttransfusionen und der dadurch ausgelösten Immunsuppression.
Zum damaligen Zeitpunkt wurde aber noch Vollblut oder Blut mit nur relativ gering abgereichertem Anteil an weißen Blutkörperchen und Blutplasma der Blutspender gegeben, welche für die immununterdrückende Wirkung hauptverantwortlich sind. Seit einigen Jahren werden nur noch rote Blutkörperchen ohne weiße Blutkörperchen (leukozytendepletiert) und weitgehend ohne Blutplasma gegeben, so dass der immununterdrückende Effekt ganz erheblich gesunken ist. Ob er noch meßbar ist, ist möglich, wird aber für die klinische Relevanz kontrovers diskutiert.
Tumorpatienten mit einem niedrigen Hämoglobin-Wert haben meist eine krankheits- oder therapiebedingte Schwäche des Knochenmarks für die Neubildung von
roten Blutkörperchen, die in der Regel nicht ausreichend mit Eiseninfusionen positiv beeinflusst werden kann oder sogar mit einer Eisenüberladung einhergeht.
In der Sendung wird vor Metastasenwachstum durch Immunsuppression gewarnt aber verschwiegen, dass z.B. der Wachstumsfaktor für die roten Blutkörperchen (EPO) auch einen fördernden Einfluss auf das Wachstum von Metastasen haben kann. Andere Alternativen zu Bluttransfusionen in dieser Situation werden im Bericht nicht genannt (und sind auch nicht bekannt), was die Sendung für Betroffene nicht wirklich hilfreich macht.
Zusammenfassend sind Bluttransfusionen zum jetzigen Zeitpunkt für viele Menschen unverzichtbar und erheblich sicherer und nebenwirkungsärmer, als sie es vor Jahren waren. Eine Therapie vieler Leukämien oder Tumorerkrankungen ist erst mit Bluttransfusionen möglich.
in Oberhausen und Dinslaken - Partnerschaft (AG Essen PR 3104) -
Bahnhofstr. 64 - 46145 Oberhausen Tel. 0208-970 422-0 - FAX: 0208-970 422-29 - mail: praxis@onkologie-oberhausen.de
Standort Dinslaken: Kreuzstr. 28 - 46535 Dinslaken - Tel. 02064-42-2545 FAX 02064-42-2738 - www.onkologie-dinslaken.de-
Impressum Datenschutzerklärung
